对制取氯气装置的改进
制取氯气装置
绿色化学的最大特点在于它是在始端就采用实现污染预防的科学手段,因而过程和终端均为零排放或零污染。基于这点,我们有效地进行了氯气制备和性质实验的绿色化改进。高中化学课本(人教版・必修)第一册第四章的实验中要用到大量的氯气。氯气有毒,并有剧烈的刺激性,人吸入少量氯气会使鼻和喉头的黏膜受到刺激,引起胸部疼痛和咳嗽,吸人大量氯气会中毒致死。因此,本文拟对实验室制取氯气的几种途径从实验原理、反应原料、实验操作以及环境保护等方面进行分析,供同仁们在实验时参考,以期达到最佳的绿色化效果
一、改进实验的目的:
1. 我们使用课本装置制氯气时,当一个集气瓶收集满之后,要换用另一个集气瓶收集,在这换瓶的时间间隔内,难免有氯气逸散出来
2.制取所需的Cl2后,气体发生装置中残余Cl2也会逸散,教室里又无通风设备,往往使老师和学生发生不同程度的中毒。为此,对实验室制取氯气的装置进行了改进。
二、试验仪器和试剂:
分液漏斗 蒸馏烧瓶 酒精灯 带铁夹的铁架台 铁圈 集气瓶 双孔胶塞 导气管 烧杯 三通玻璃导管 10ml注射器 MnO2 浓盐酸 NaOH 溶液
三、实验仪器装置图及仪器的组装说明:
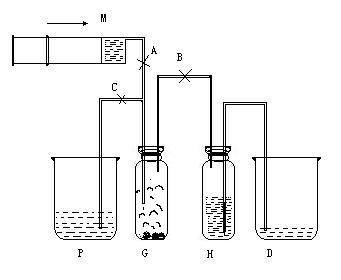
其中,蒸馏烧瓶处的双孔塞中的一孔插入一长约为10厘米的玻璃管,用乳胶管套住,图中玻璃导气管连接处用止水夹A、B、C将乳胶管夹住

四、实验操作部分:
1. 实验开始时,将A、B 两处止水夹关闭,打开C处止水夹,加热,待烧杯中导气管出口处的气泡连续均匀发出时,将C关闭,打开B,集气管即可收集到Cl2;
2. 当Cl2集满后(可观察黄绿色气体是否充满集气瓶),打开C,关闭B,Cl2可通过导气管进入烧杯中被NaOH溶液吸收。
3.再继续收集时,又可打开B关闭C;
4. 所需的Cl2收集好后,关闭B和C,移走酒精灯。将吸有15% NaOH溶液的注射器插入A处乳胶管内,打开A处止水夹,使 NaOH 溶液进入烧瓶中,以中和没有反应的盐酸和吸收瓶内残留的Cl2 。因一次滴入 NaOH 溶液的量不够,故要再加入2或3次,当加入NaOH溶液时应关闭A,否则仍有 Cl2 从A处逸出。
五、装置改进的意义:
其一, 更换集气瓶时,不须撤离酒精灯,可连接操作;其二,尾气始终被 NaOH 溶液吸收,设备简单,操作方便,无丝毫污染;其三, 反应发生装置中残留的Cl2 被 NaOH 溶液吸收,有效的控制了Cl2的扩散;其四,上述制气装置也可用于SO2的制取。
§1.2氯气与水、碱反应装置的绿色化
为了防止Cl2和水、碱反应时气体外逸,对环境造成污染,我们对实验进行了如下改进:
实验仪器 医用注射器(50ml)、矿泉水瓶(550ml)、橡皮塞。
操作步骤:①收集一矿泉水瓶Cl2,用橡皮塞塞紧。②用注射器吸取50ml左右的水从橡皮塞处注入瓶中,振荡瓶子。③用注射器吸取少量紫色石蕊溶液从橡皮塞处注入该瓶中。④最后用注射器吸取10ml左右的NaOH溶液也从橡皮塞处注入该瓶中,振荡瓶子
优点:①安全可靠,无污染。②取材方便,做到了废物利用,节省了资金。
③装置简单,操作方便,现象明显。④本实验不仅可以验证Cl2与水、碱的反应,也能确定氯水的成分和物理性质,一举多得,节约了原料。